机构名称:
¥ 1.0
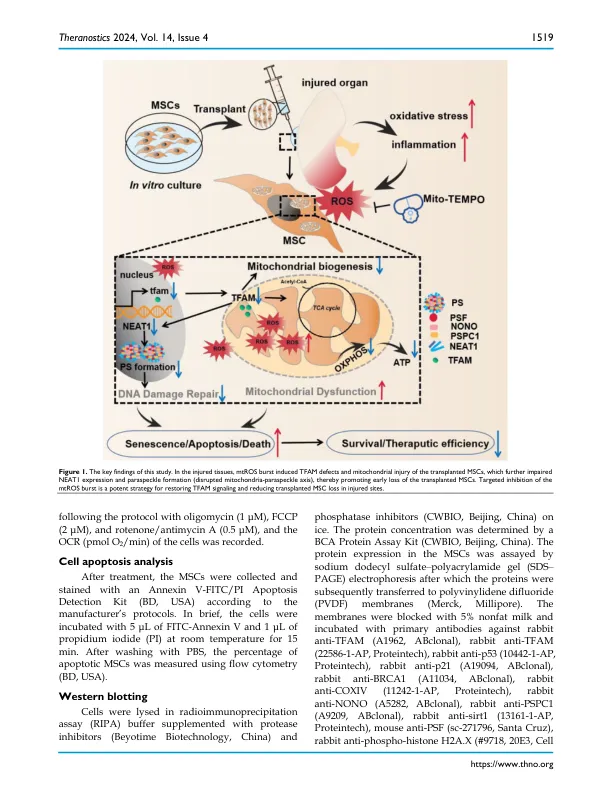
原理:基于干细胞的疗法已成为组织工程和再生医学的有前途的工具,但是它们的治疗疗效在很大程度上受到氧化应激诱导的受伤组织部位移植细胞的丧失的限制。为了解决这个问题,我们旨在探索ROS引起的MSC损失的潜在机制和保护策略。方法:使用实时PCR,Western blotting和RNA测序评估了TFAM(线粒体转录因子A)信号传导,线粒体功能,线粒体损伤,DNA损伤,凋亡和衰老。还分析了MSC中TFAM或LNCRNA核拼接组件的转录本1(Neat1)敲低或过表达对线粒体功能,DNA损伤修复,凋亡和衰老的影响。在肾脏缺血/再灌注(I/R)损伤的小鼠模型中评估了线粒体靶向抗氧化剂(mito-tempo)对移植MSC存活的影响。结果:线粒体ROS(MTROS)爆发导致TFAM信号传导和总体线粒体功能的缺陷,这进一步损害了Neat1表达及其介导的副夹层的形成和MSC中的DNA修复途径,从而在氧化应激下共同促进MSC衰减和死亡。相比之下,有针对性的抑制MTROS爆发是一种足够的策略,可以减轻受伤组织部位的早期移植MSC损失,而Mito-Tempo的共同给药可改善移植的MSC的局部保留和减少缺血性肾脏的氧化损伤。结论:本研究确定了线粒体 - 拼双轴在调节细胞存活中的关键作用,并可能为开发用于组织工程和再生医学的先进干细胞疗法提供见解。
线粒体 - 覆盖轴轴调节生存...
主要关键词