机构名称:
¥ 1.0
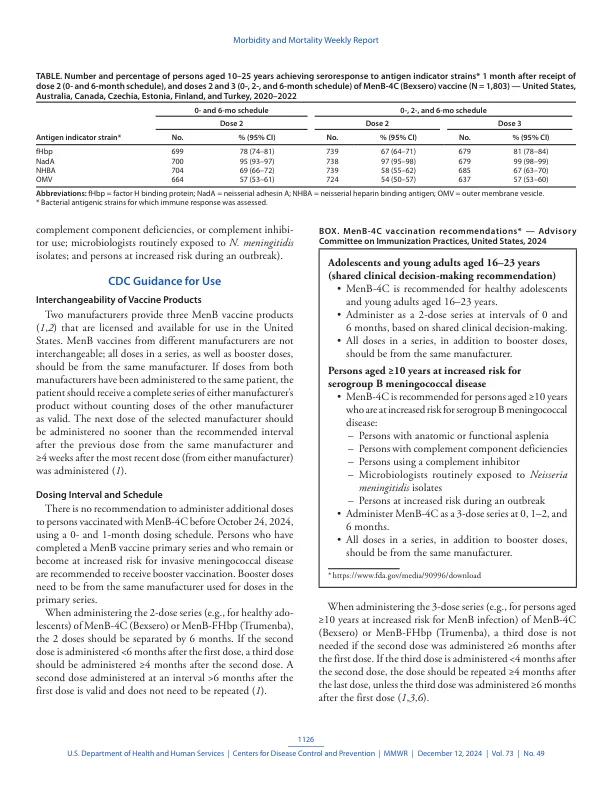
摘要 两种 B 群脑膜炎球菌疫苗已获准在美国使用。2024 年 8 月,美国食品药品监督管理局 (FDA) 根据新的免疫原性数据,将 B 群脑膜炎球菌 MenB-4C 疫苗 (Bexsero) 的标签从 2 剂接种方案(间隔 0 和 ≥1 个月)更改为 2 剂接种方案(0 和 6 个月),并增加了 3 剂接种方案(0、1-2 和 6 个月)。2024 年 10 月 24 日,免疫实践咨询委员会 (ACIP) 投票决定更新其对 MenB-4C 给药间隔和接种方案的建议,以符合新的 FDA 标签。 ACIP 建议,基于共同临床决策,将 16-23 岁健康青少年和青年人 MenB-4C 2 剂系列接种间隔从 0 和 ≥1 个月延长至 0 和 6 个月,并增加了 3 剂系列接种建议,即针对 10 岁以上高风险人群,分别在 0、1-2 和 6 个月接种剂量。ACIP 更新的 MenB-4C 建议与现有的 ACIP 针对其他 FDA 批准的 B 群脑膜炎球菌疫苗 MenB-FHbp (Trumenba) 的建议一致。
Bexsero MenB 的新给药间隔和时间表 - ...