机构名称:
¥ 1.0
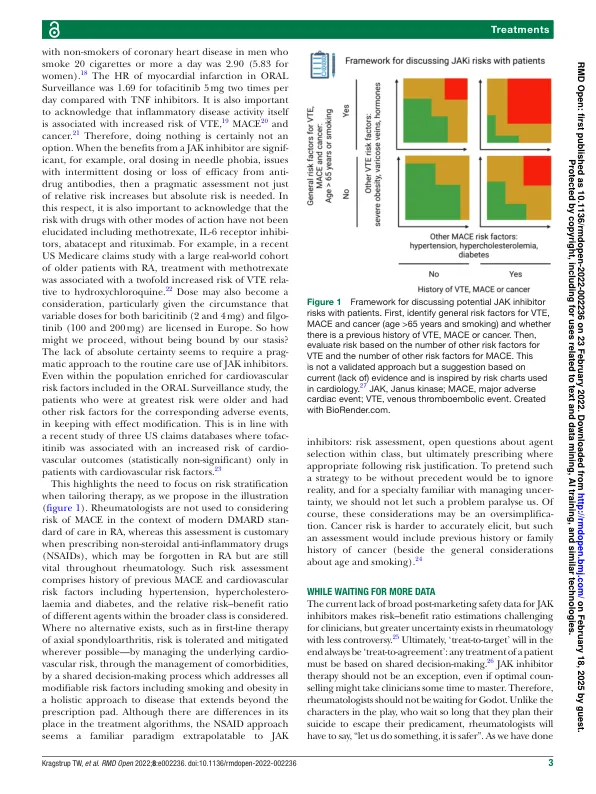
摘要 美国食品药品管理局 (FDA) 最近在所有目前获批的用于治疗关节炎和其他炎症疾病的 Janus 激酶 (JAK) 抑制剂上添加了新的“黑框警告”,该警告基于托法替尼与肿瘤坏死因子 α 抑制剂在类风湿性关节炎中的 ORAL 监测研究结果。这个警告很难被忽视,因为数据来自随机对照试验,保真度高,很难指责。这尤其成问题,因为所有其他 JAK 抑制剂的安全性数据都将在几年内待定。那么,我们该如何继续,不受停滞状态的束缚?缺乏绝对确定性似乎需要对 JAK 抑制剂的常规护理使用采取务实的方法。风险最大的患者年龄较大,并且有相应不良事件的其他风险因素,以符合效果修改。这凸显了在制定治疗方案时需要关注风险分层。从这个角度来看,我们提出了一个简单的例子来指导临床决策。首先,确定静脉血栓栓塞事件 (VTE)、重大不良心脏事件 (MACE) 和癌症的一般风险因素(年龄>65 岁且吸烟),以及是否有 VTE、MACE 或癌症病史。然后,根据 VTE 的其他风险因素数量和 MACE 的其他风险因素数量评估风险。最终,“按目标治疗”最终将始终是“按协议治疗”。正如我们过去所做的那样,未来也将如此,最佳治疗策略必须根据患者个人的风险因素和偏好在共同决策过程中量身定制。
等待JAK抑制剂安全数据
主要关键词