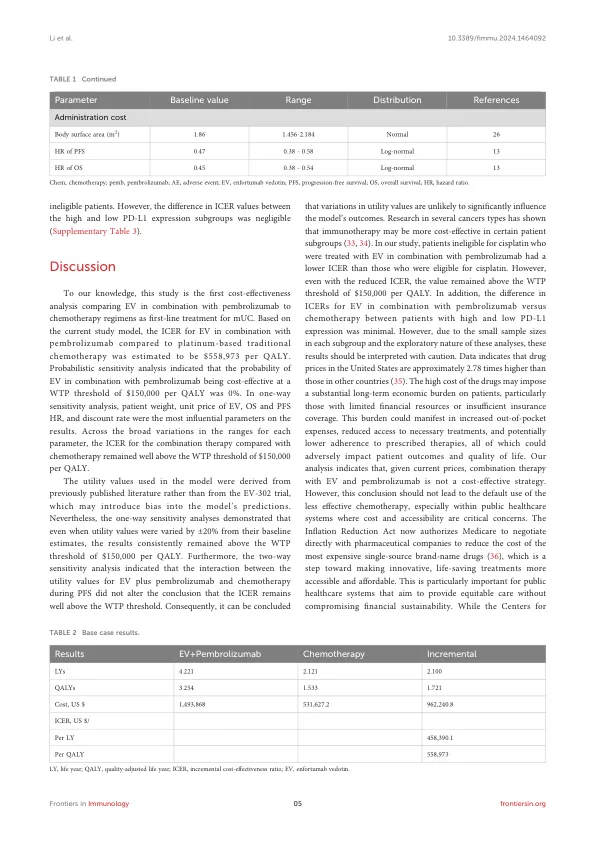
膀胱癌是美国十种最常见的癌症之一,占2023年所有新癌症病例的4.2%(1)。约90-95%的膀胱癌病例是尿路上皮癌(2,3)。转移性尿路上皮癌(MUC)的预后较差,五年生存率仅为5-7%(1)。基于铂的化学疗法是先前未经治疗的MUC患者的护理标准(4),但是,与该方案相关的临床结果仍然是最佳的(5)。免疫疗法在癌症治疗领域变得越来越流行,因为它的出色效率在治疗乳腺癌和甲状腺癌(6,7)中。PD-1和PD-L1抑制剂通常用于不符合铂基化学疗法的患者,作为基于铂的化学疗法后的后续疗法,或作为复发或抗性病例的替代疗法(8)。尽管在MUC中使用了这些抑制剂,但许多患者仍经历进展(9)。Enfortumab Vedotin(EV),一种针对Nectin-4(10)的抗体 - 药物结合物,于2018年(11)在美国食品药物管理局(FDA)(11)中获得了突破性疗法名称,随后于2019年12月获得了营销批准,以其在MUC患者中用作第二线治疗(12)。与化学疗法相比,接受EV和pembrolizumab的患者的生存率显着,将死亡的风险降低了53%,总中位生存率(OS)降低了,危险比(HR)(HR)为0.47(中位数OS:31.5个月VS. 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9 16.9。适用于先前接受过基于铂的化学疗法和免疫检查点抑制剂(ICI)治疗的局部晚期或转移性膀胱癌的患者,并建议使用NCCN指南(8)使用其用于MUC的二线治疗。EV-302试验评估了EV和Pembrolizumab和Pembrolizumabed患者的组合(13)。联合疗法还将进展或死亡的风险降低了55%,中位PFS几乎翻了一番,HR为0.45(中位PFS:12.5个月,而6.3个月)。基于这些结果,FDA已批准EV和Pembrolizumab作为MUC患者的第一线治疗(14)。尽管该试验表明中位OS和PF的同时几乎增加了一倍,但从价值的角度来看,该疗法的成本是否通过其潜在的好处来恰当地尚不清楚。这项研究的目的是评估EV与Pembrolizumab与基于铂的化学疗法的成本效益,从美国付款人的角度来看,MUC患者的第一线治疗。
第一行Enfortumab Vedotin在...
主要关键词