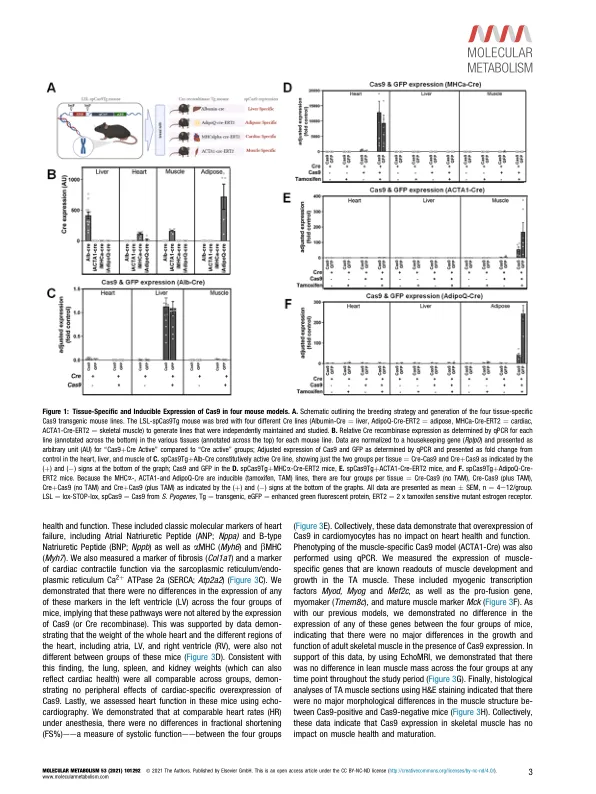
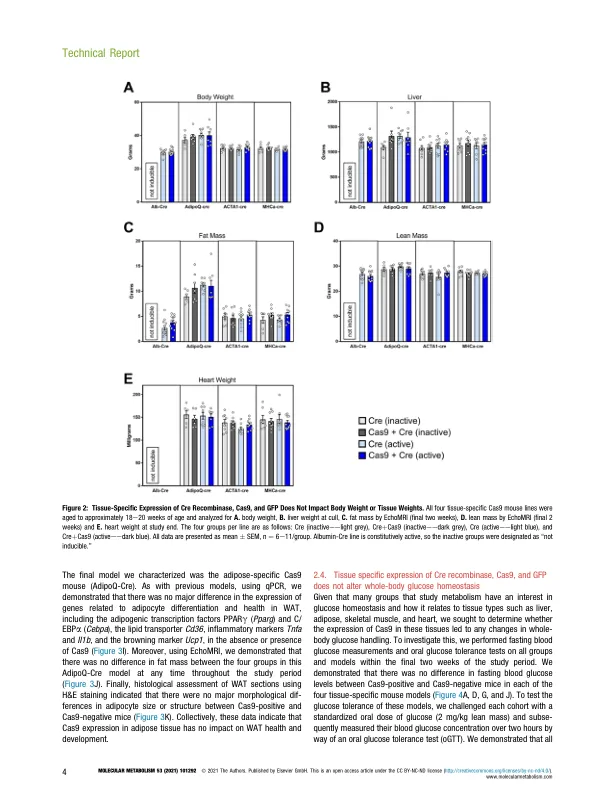
目标:CRISPR/Cas9 技术彻底改变了基因编辑,并加快了我们操纵目标基因的能力,以造福研究和治疗应用。尽管该领域已经取得了许多进展,并且还在继续取得进展,但迄今为止使用最广泛的技术可能是产生敲除细胞、组织和动物。该技术的优势是多方面的,但关于长期表达 Cas9 等外来蛋白质对哺乳动物细胞功能的影响,仍然存在一些问题。几项研究表明,Cas9 的慢性过度表达(无论是否伴有其伴随的向导 RNA)可能会对细胞功能和健康产生有害影响。在体内应用该技术时,这一点尤其令人担忧,因为 Cas9 在目标组织中的慢性表达可能会促进疾病样表型,从而混淆对目标基因影响的研究。尽管这些担忧仍然存在,但据我们所知,尚无任何研究直接证明这一点。方法:在本研究中,我们使用 lox-stop-lox (LSL) spCas9 ROSA26 转基因 (Tg) 小鼠系生成了四种组织特异性 Cas9-Tg 模型,这些模型在心脏、肝脏、骨骼肌或脂肪组织中表达 Cas9。我们对这些小鼠进行了全面的表型分析,直至 20 周龄,随后对其器官进行了分子分析。结果:我们证明 Cas9 在这些组织中的表达对动物的全身健康没有不利影响,也不会对全身能量代谢、肝脏健康、炎症、纤维化、心脏功能或肌肉质量产生任何组织特异性影响。结论:我们的数据表明,这些模型适用于使用 LSL-Cas9-Tg 模型研究基因缺失的组织特异性效应,并且利用这些模型观察到的表型可以自信地解释为基因特异性的,并且不会因 Cas9 的慢性过表达而混淆。2021 作者。由 Elsevier GmbH 出版。这是一篇根据 CC BY-NC-ND 许可协议开放获取的文章(http://creativecommons.org/licenses/by-nc-nd/4.0/)。
Cas9 的组织特异性表达对整体没有影响......