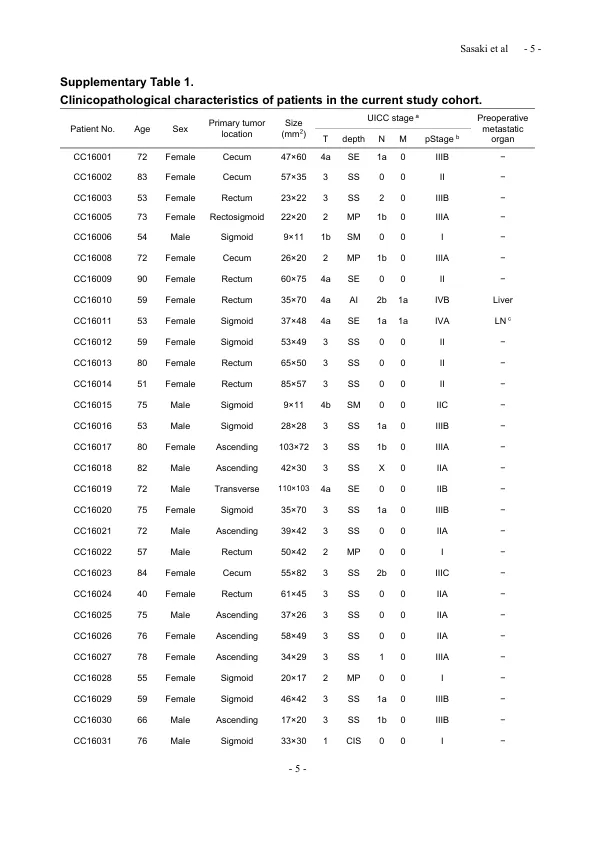
手术获得的原发性肿瘤组织样品和相应的连续血样品,分别获得了体细胞突变筛查和ctDNA监测。使用三组结直肠癌患者(CRC)的三个不同平台对原发性肿瘤进行了测序分析。分别分析了11、27和14例患者的肿瘤样本,分别为1、2和3组。使用Clearseq综合癌症小组(Agilent Technologies,Inc.,Santa Clara,CA)使用Illumina HISEQ 2000 Sequencer(Illumina,Inc。,San Diego,CA)分析集1,该基因针对151个疾病相关的基因(Maintext的参考文献34)。 分别使用ION Proton™和ION S5™系统(Thermo Fisher Scientific,Waltham,MA)分析了集2和3,其定制面板的靶向39个基因,这些基因经常在CRC中改变。 1集1样品在我们的先前研究中进行了分析,该研究考虑了原发性肿瘤的三个区域以及外周血单核细胞(PBMCS)(总共四个样品)的相应DNA,以评估肿瘤内遗传异质性对循环肿瘤DNA DNA(CTDNA)(CTDNA)(参考文本34)的影响。 在该研究中,结果表明,肿瘤遗传异质性并不是CTDNA分析的主要障碍,前提是从肿瘤的单个区域中选择具有足够变异等位基因频率(VAF)的体突变。 本研究中原发性肿瘤测序的最高优先级是检测一些具有高VAF的体细胞突变。集1,该基因针对151个疾病相关的基因(Maintext的参考文献34)。集2和3,其定制面板的靶向39个基因,这些基因经常在CRC中改变。1集1样品在我们的先前研究中进行了分析,该研究考虑了原发性肿瘤的三个区域以及外周血单核细胞(PBMCS)(总共四个样品)的相应DNA,以评估肿瘤内遗传异质性对循环肿瘤DNA DNA(CTDNA)(CTDNA)(参考文本34)的影响。在该研究中,结果表明,肿瘤遗传异质性并不是CTDNA分析的主要障碍,前提是从肿瘤的单个区域中选择具有足够变异等位基因频率(VAF)的体突变。本研究中原发性肿瘤测序的最高优先级是检测一些具有高VAF的体细胞突变。此外,三个肿瘤区域中通常检测到的突变仅限于一组基因,其中包括TP53,APC,KRAS,PIK3CA,FBXW7和BRAF。
补充材料