机构名称:
¥ 1.0
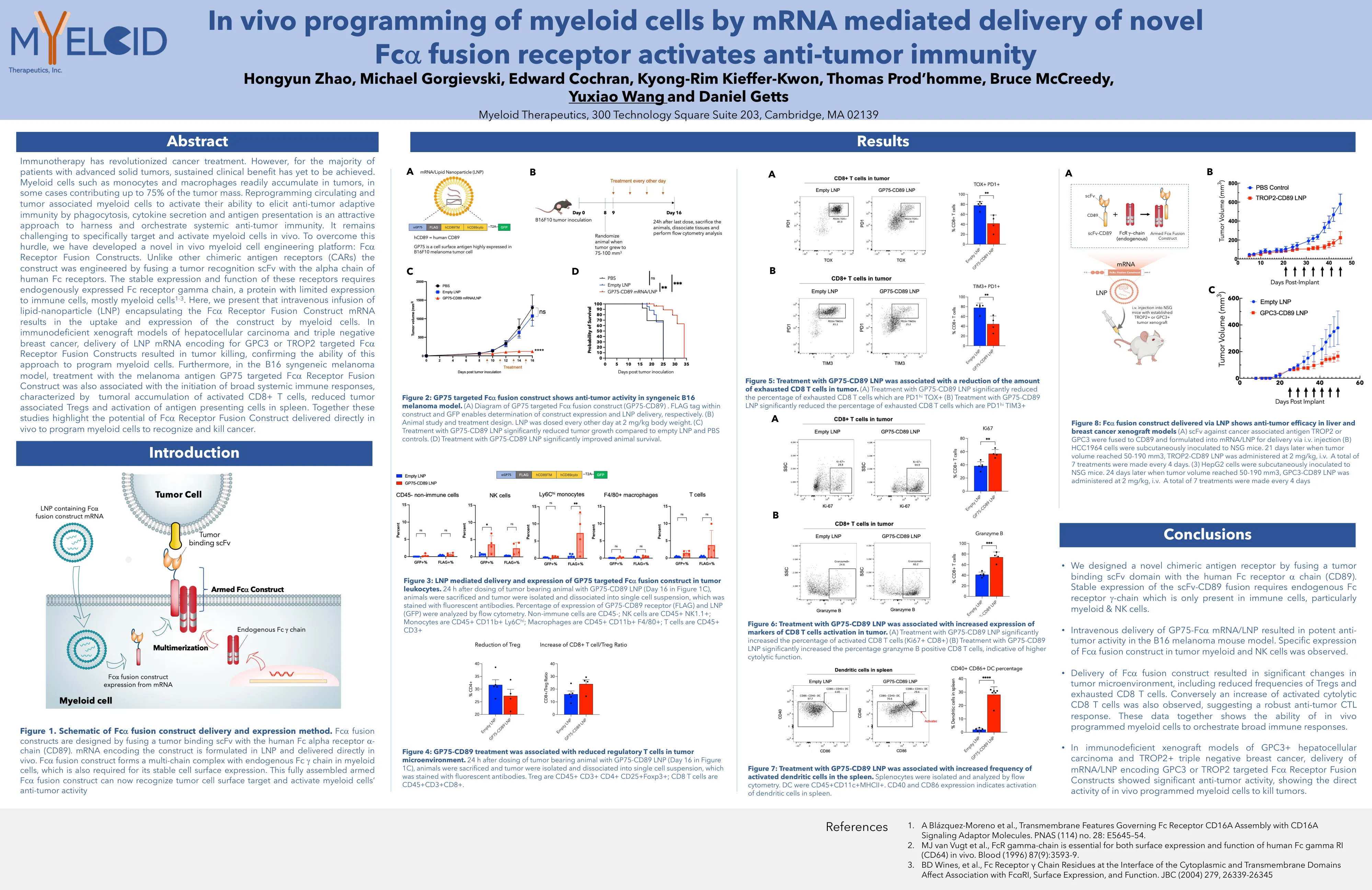
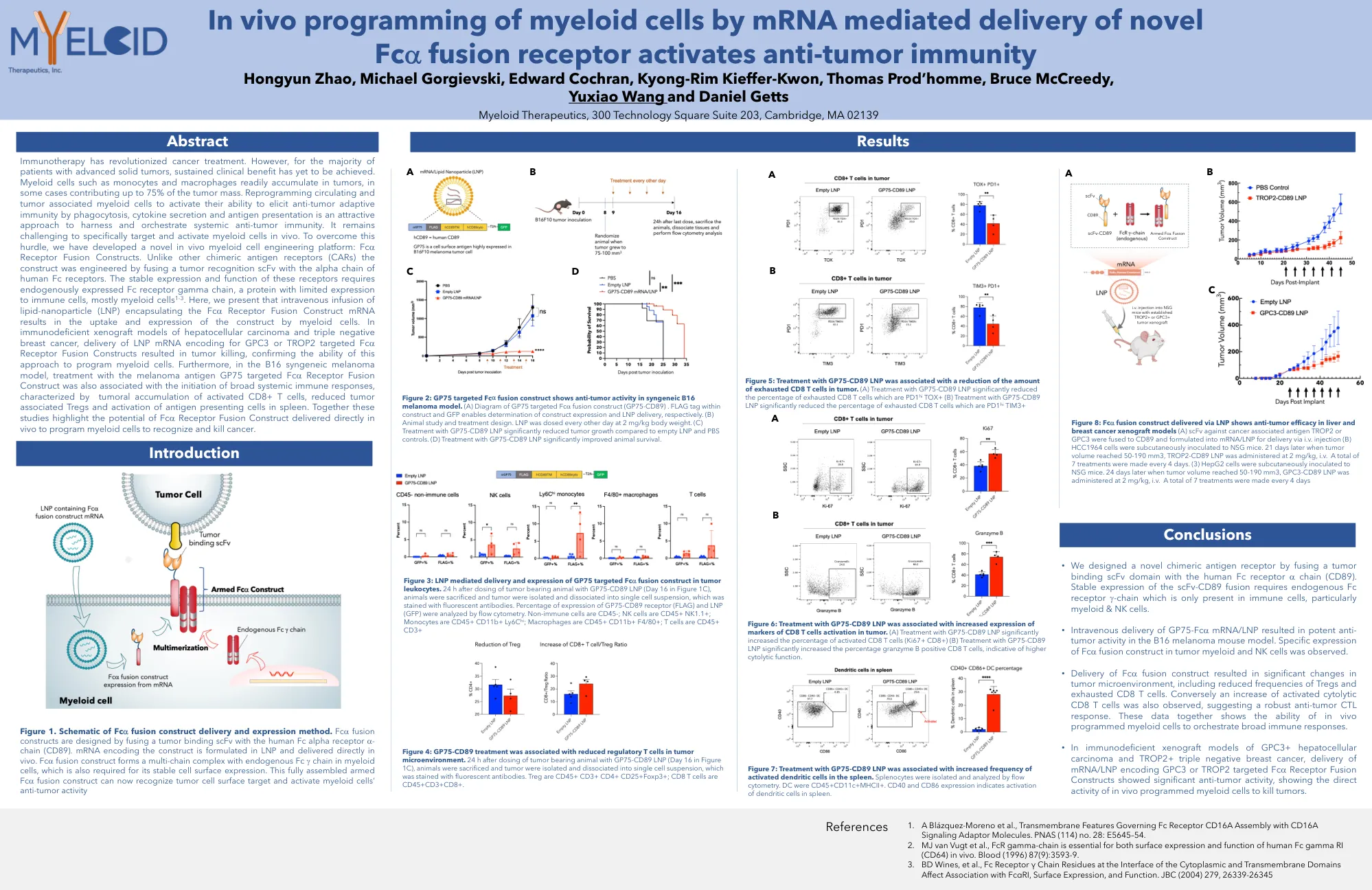
免疫疗法彻底改变了癌症治疗。但是,对于大多数晚期实体瘤患者,尚未实现持续的临床益处。髓样细胞(如单核细胞和巨噬细胞)很容易积聚在肿瘤中,在某些情况下,肿瘤质量的75%。重编程循环和肿瘤与髓样细胞相关,以激活其通过吞噬作用,细胞因子分泌和抗原表现来激活抗肿瘤适应性免疫的能力,是一种有吸引力的方法,可利用并策划系统性的抗肿瘤免疫。在体内专门靶向和激活髓样细胞仍然具有挑战性。为了克服这一障碍,我们开发了一种新型的体内髓细胞工程平台:FC A受体融合构建体。与其他嵌合抗原受体(CAR)不同,该构建体是通过将肿瘤识别SCFV与人体FC受体的α链融合而设计的。这些受体的稳定表达和功能需要内源表达的FC受体γ链,FC受体γ链是一种对免疫细胞表达有限的蛋白质,主要是髓样细胞1-3。在这里,我们介绍了包裹FC A受体融合构建体mRNA的静脉输注脂质 - 纳米颗粒(LNP)导致髓样细胞对构建体的摄取和表达。在肝细胞癌和三重阴性乳腺癌的免疫缺陷异种移植模型中,针对GPC3或trop2靶向FC的LNP mRNA的递送A受体融合构建体导致肿瘤杀死,从而确认了这种方法为骨髓细胞编程的能力。此外,在B16合成性黑色素瘤模型中,用黑色素瘤抗原GP75靶向FC A受体融合构建体的治疗也与启动广泛的全身免疫反应的启动有关,其特征在于肿瘤积累活化的CD8+ T细胞,可减少与肿瘤相关的TREG和SpleeNing spleen and spleen spleen and spleen的活化。这些研究共同强调了FC A受体融合构建体的潜力,直接在体内传递以编程髓样细胞以识别和杀死癌症。
AACR2022体内递送海报
主要关键词