机构名称:
¥ 1.0
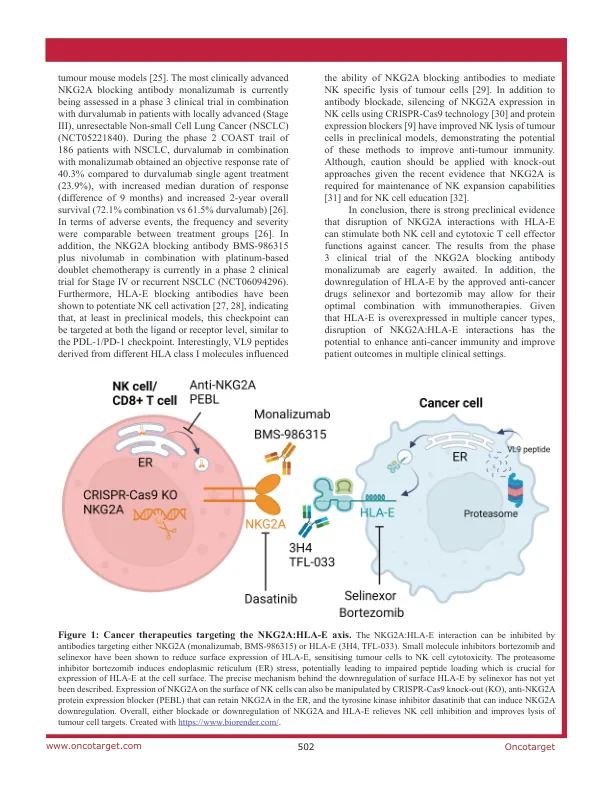
抑制性受体NKG2A与CD94形成异二聚体,由〜50%的外周血NK细胞表达,并在NK细胞扩张后进一步上调[1]。此外,NKG2A是CD8+ T细胞上的晚期免疫检查点,在反复的抗原刺激和分裂后,它上调了[2]。NKG2A在耗尽的CAR T细胞上还发现了27天的T细胞输注[3]和CD8+肿瘤浸润T细胞[4-6]。有趣的是,NKG2A具有有效的抗肿瘤活性[7]。NKG2A通过其配体HLA-E的参与导致磷酸酶的募集和激活,这些磷酸酶抑制了NK细胞和T细胞激活[8]。 与健康组织相比,在多种癌症中高度表达了 HLA-E [4,9],并且已证明通过HLA-E逃避NK和CD8+ T细胞免疫[10]。 两项在癌细胞中采用CRISPR筛查的研究确定HLA-E是NK细胞的关键负调节剂:癌细胞相互作用[11,12]。 根据此,IFNγ信号传导与STAT1激活增加和HLA-E表达增强引起的NK细胞电阻有关[11]。 这在HLA-E的鼠同源物QA-1B也很明显,QA-1B的鼠同源物在所有测试的细胞类型上被炎症信号上调[13]。NKG2A通过其配体HLA-E的参与导致磷酸酶的募集和激活,这些磷酸酶抑制了NK细胞和T细胞激活[8]。HLA-E [4,9],并且已证明通过HLA-E逃避NK和CD8+ T细胞免疫[10]。两项在癌细胞中采用CRISPR筛查的研究确定HLA-E是NK细胞的关键负调节剂:癌细胞相互作用[11,12]。根据此,IFNγ信号传导与STAT1激活增加和HLA-E表达增强引起的NK细胞电阻有关[11]。这在HLA-E的鼠同源物QA-1B也很明显,QA-1B的鼠同源物在所有测试的细胞类型上被炎症信号上调[13]。
HLA-E相互作用可改善抗癌免疫力
主要关键词