机构名称:
¥ 1.0
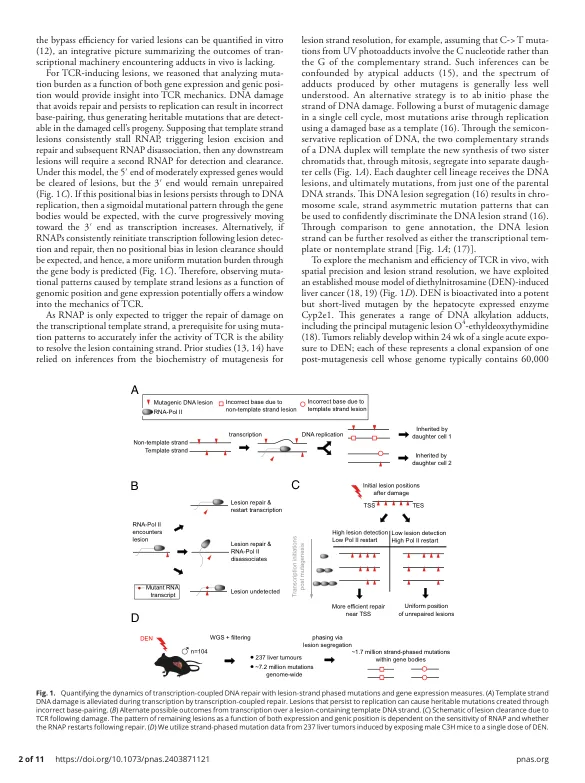
DNA碱基损伤是致癌突变和基因表达中断的主要来源。RNA聚合酶II(RNAP)在DNA损伤部位的失速和随后的修复过程触发在塑造基因组 - 突变的广泛分布,清除转录障碍以及最小化错误编码的基因产物的过程中具有重要作用。尽管对遗传完整性的重要性很重要,但这种转录耦合修复(TCR)过程的关键机理特征是限制或未知的。在这里,我们利用了一个井中的体内哺乳动物模型系统,以探索TCR的机械性能和参数,以良好的空间分辨率以及损坏的DNA链的区分,以烷基化损伤。为了进行严格的解释,开发了DNA损伤和TCR的可推广数学模型。将实验数据拟合到模型,模拟表明RNA聚合酶经常绕过不触发修复的病变,表明小烷基化加合物不太可能是基因表达的有效障碍。损害爆发后,转录 - 耦合修复的效率逐渐通过基因体衰减,对癌症驱动器突变的发生和准确推断的影响。重新修复修复位点的转录不是转录的一般特征 - 耦合修复,并且观察到的数据与重新定期永远不会发生。共同揭示了TCR的方向性但随机活性如何塑造DNA损伤后突变的分布。
DNA病变旁路和转录耦合修复的随机动力学
主要关键词