机构名称:
¥ 1.0
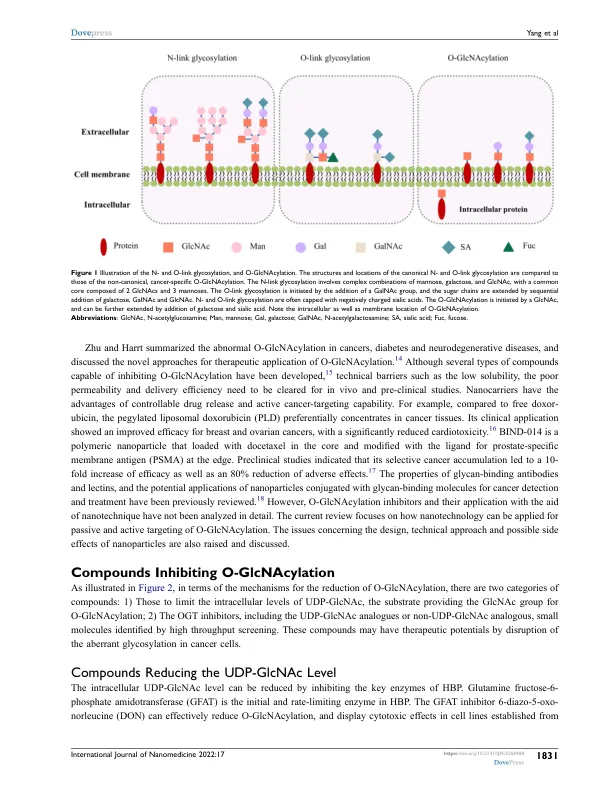
摘要:越来越多的数据表明,多种癌症的细胞表面和细胞内的蛋白质O-GlcNAc糖基化增加。异常的O-GlcNAc糖基化被认为是潜在的治疗靶点。尽管已经开发出多种能够抑制O-GlcNAc糖基化的化合物,但其溶解性低、渗透性和递送效率差阻碍了其在体内和临床前研究中的应用。纳米载体具有可控药物释放和主动靶向癌症的能力。此外,纳米粒子可以通过增强癌症中的渗透性和保留(EPR)效应来提高药物递送效率并减少正常组织中的非特异性分布。利用O-GlcNAc特异性抗体或凝集素,纳米粒子可以进一步提高其癌症靶向能力。尽管针对典型 N 和 O 连接糖基化的纳米载体已被广泛研究用于癌症检测和治疗,但尚未积极应用纳米技术来特异性靶向 O-GlcNAc 化。本综述总结了 GlcNAc 化及其在癌症中的改变的一般特征。分析集中在以下领域:纳米载体如何改善 O-GlcNAc 转移酶 (OGT) 抑制剂的溶解度和/或细胞通透性;用凝集素或抗体修饰纳米载体以主动靶向 O-GlcNAc;纳米载体介导的 OGT 抑制剂和常规药物的共同递送,这可能导致协同效应。还讨论了阻碍 O-GlcNAc 化靶向方案研究进展的未解决问题。关键词:O-GlcNAc 化、纳米载体、OGT 抑制剂、靶向治疗、凝集素、联合治疗
纳米技术如何使 O-GlcNAcylation 焕发活力 - ...
主要关键词