机构名称:
¥ 1.0
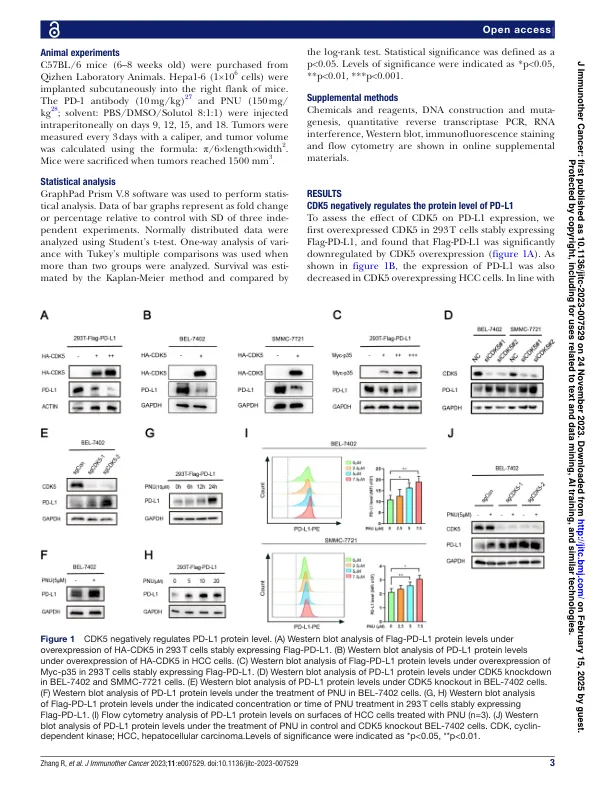
摘要 背景 在过去的几年中,针对程序性细胞死亡蛋白 1 (PD-1) 及其配体程序性细胞死亡配体 1 (PD-L1) 的肝细胞癌 (HCC) 免疫疗法已经取得了持久的临床效益。然而,仅有一小部分 HCC 患者对单独 PD-1/PD-L1 阻断表现出客观的临床反应。尽管对 PD-L1 翻译后修饰的影响很大,但其在 HCC 免疫疗法耐药性中的意义仍不甚明了。方法 在 HCC 细胞中敲低细胞周期蛋白依赖性激酶 5 (CDK5) 表达,用蛋白质印迹法检测 CDK5 和 PD-L1 蛋白水平。进行免疫共沉淀以评估蛋白质之间的相互作用。构建临床前 HCC 小鼠模型以评估 CDK5 抑制剂单独或与 PD-1 抗体联合使用的效果。使用临床HCC样本阐明CDK5、PD-L1和PD-L1 T290磷酸化在HCC中的临床意义。结果我们发现CDK5缺陷会上调HCC细胞中PD-L1蛋白的表达,并揭示出一种PD-L1被CDK5下调的新型分子机制,即CDK5介导的T290位PD-L1磷酸化促进其与伴侣蛋白热休克同源蛋白70(HSC70)结合并通过伴侣介导的自噬进行降解。值得注意的是,CDK5抑制剂PNU112455A治疗可有效上调肿瘤PD-L1水平,促进对抗PD-1免疫治疗的反应,并延长HCC肿瘤小鼠的生存时间。此外,PD-L1的T290磷酸化状态与HCC的预后相关。结论 靶向CDK5可与PD-1阻断协同抑制HCC生长,可能具有临床益处。本研究揭示了HCC中PD-L1降解的独特调控,为HCC的临床治疗提供了一个有吸引力的治疗靶点、一种潜在的药物和一种新的预后指标。
CDK5 通过分子伴侣破坏 PD- L1
主要关键词