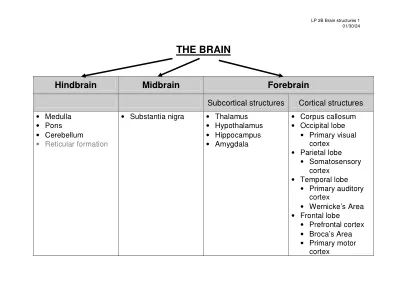
与其他国家(尤其是美国)形成鲜明对比的是,只有有限数量的保险公司用重复的经颅杂志刺激(RTMS)偿还治疗,而没有经跨颅电气刺激(TES)。因此,欧洲非侵入性脑刺激(NIB)的研究和临床降低的治疗可用性和投资将落后。出乎意料的是,突然不受欢迎的监管变化使欧洲局势变得更糟。在2022年12月,欧盟重新分类的RTM和低强度TE作为III类,最高风险类别(https://eur-eur-lex.europa.eu/eli/eli/eli/eg_impl/2022/2347/oj)。在先前的监管框架(医疗设备指令,MDD)下,欧盟并未具体规定调节NIBS设备,但大多数人被分类为IIA类(可管理的风险,批准的治疗效果)。III类设备(例如深脑刺激植入物)被定义为侵入性,因为它们直接连接到循环系统或中枢神经系统。尽管这种新的重新分类目前仅是“没有预期的医疗目的的产品”(对于许多研究人员和医生不清楚的术语),这是关于RTMS和TES的风险和不利影响的证据 - 这是这种恢复性的综合性 - 非常有效的 - 非常适合。欧盟显然评估了NIBS对患者的安全构成比以前想象的更大的风险。据称TMS/TE可以诱导“非典型大脑发育”或“脑活动的异常模式”)。此评估是基于与可用科学证据相矛盾的RTM和低强度TE的错误陈述,许多既定的主张和假设都是错误的(例如,同样,根据实际临床数据,对RTMS/TES相关的癫痫发作风险的显着提及与该领域中最新的共识声明相矛盾,这表明观察到的癫痫发作率远低于以前的指南。先前关于癫痫发作风险的谨慎不再得到科学证据的支持[1,2]。如何建立该欧盟裁决是很难理解的。显然,在2021年5月,引入了一项新的医疗设备法规(MDR),并专门针对附件XVI的非医疗用途提出了NIBS。MDR的应用将通过“过渡期”(第120条)逐渐发展,直到2024年5月,这意味着只要遵守过渡规则,就可以允许现有的NIBS产品(来自先前MDD的I类和IIA类的IIA)一直保持在市场结束。
大脑刺激
主要关键词