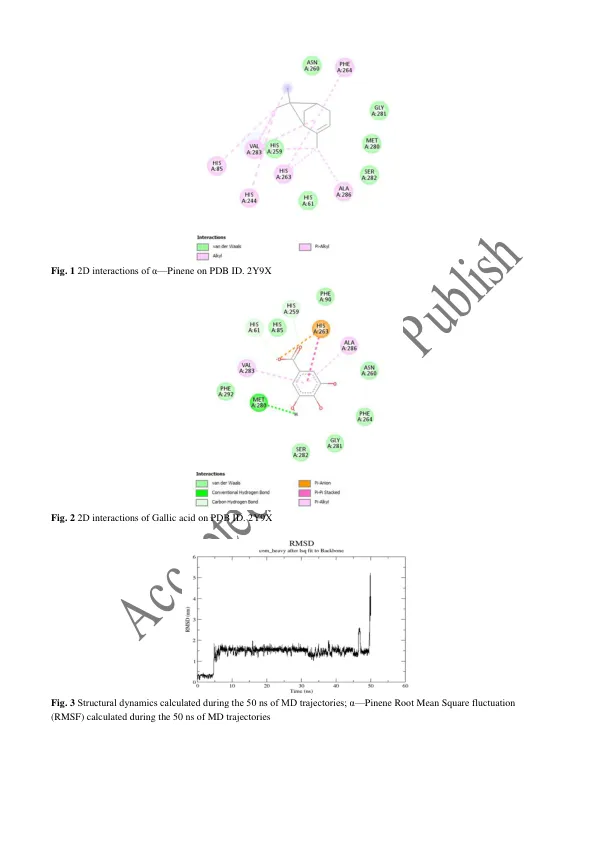
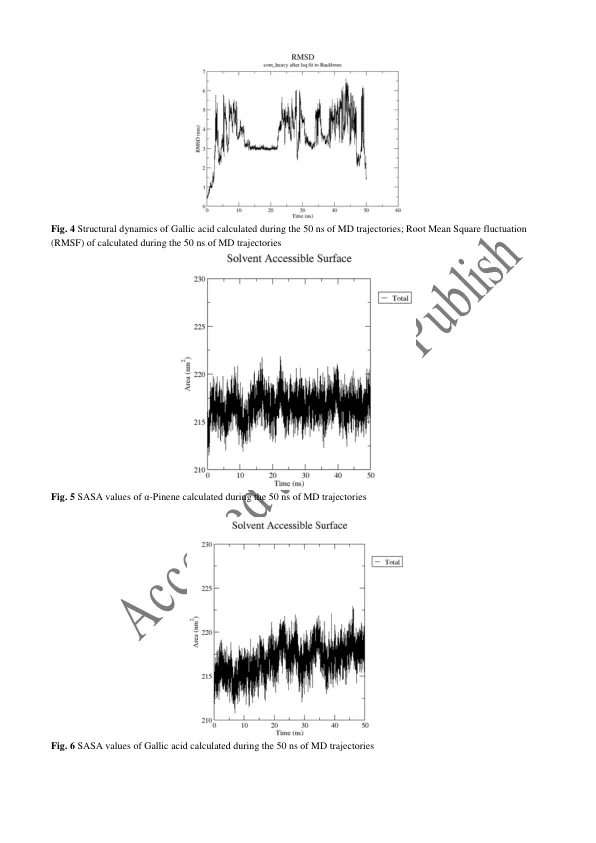
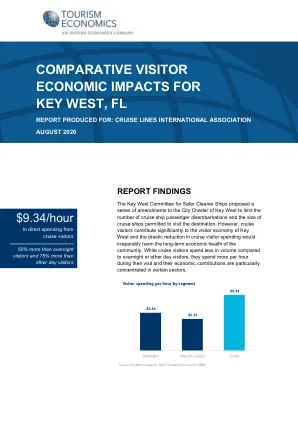
文章历史:收到日期:2024 年 9 月 12 日/接受修订版日期:2024 年 11 月 16 日 © 2012 伊朗药用植物协会。保留所有权利 摘要 酪氨酸酶是黑色素合成的关键酶。因此,许多酪氨酸酶抑制剂已经在化妆品和药物中进行了测试。本研究的目的是比较没食子酸和 α-蒎烯的抗酪氨酸酶潜力。初步分析是使用分子对接方法进行的。然后,使用蘑菇酪氨酸酶进行实验室实验,以儿茶酚为底物,曲酸为酶的标准抑制剂。使用 DPPH 自由基评估没食子酸和 α-蒎烯的抗氧化活性。对接得分显示没食子酸对酪氨酸酶具有强结合亲和力(ΔG = -6.33 Kcal/mol),与Met 280形成H键,与His 263形成π-π堆积。α-蒎烯只能通过疏水相互作用与活性口袋结合,导致结合亲和力较低(ΔG = -3.89 Kcal/mol)。没食子酸表现出最高的抑制效果(IC 50 = 0.130 mg/mL),而α-蒎烯表现出较低的抑制能力(IC 50 = 0.392 mg/mL)。抑制类型为曲酸的竞争性抑制和没食子酸的非竞争性抑制。在DPPH自由基清除测试中,没食子酸和α-蒎烯的EC 50值分别为0.269 mg/mL和251.2 mg/mL。计算机模拟和实验室结果几乎相同。尽管 α-蒎烯对酪氨酸酶的抑制剂作用不如没食子酸强,但增加其浓度或许可以增强其作用。没食子酸的抗氧化潜力明显高于 α-蒎烯,因此从这个角度来看,没食子酸更无害,安全性更高。 关键词:酪氨酸酶,α-蒎烯,没食子酸,黑色素 引言 酪氨酸酶 (EC 1.14.18.1) 属于 3 型含铜蛋白家族 [1]。保守活性位点中的两个铜离子 Cu-A 和 Cu-B 由 6 个组氨酸残基配位 [2]。酪氨酸酶也是节肢动物角质层形成和植物褐变的重要因素 [3]。它还参与伤口愈合、紫外线防护和酚类解毒 [4]。酪氨酸酶和氧化酶一样,是许多生物体黑色素生成的基本酶,对色素沉着至关重要。催化 L-酪氨酸转化为 L-多巴是黑色素形成酶促途径的限速步骤 [5]。1895 年,Bourquelot 和 Bertrand 首次从蘑菇中分离出酪氨酸酶。此后,酪氨酸酶已从多种细菌、真菌、植物和动物来源中分离和纯化。酪氨酸酶的结构包含三个结构域:N 端、中心和 C 端结构域 [6]。酪氨酸酶抑制剂种类繁多,其中大多数已用商业蘑菇酪氨酸酶进行测试,与哺乳动物酪氨酸酶相矛盾。然而,最近的研究报告显示,蘑菇酪氨酸酶和人类酪氨酸酶的抑制剂效果存在显著差异 [7]。几种酪氨酸酶抑制剂的抑制效果表明,抗坏血酸是人类酪氨酸酶和蘑菇酪氨酸酶的最佳抑制剂,并且以最低 IC 50 值来衡量 [8]。对苯二酚、曲酸和熊果苷是最著名的酪氨酸酶抑制剂,但它们具有严重的副作用,例如永久性脱色、红斑和接触性皮炎 [9]。此外,Chiari 等人对来自阿根廷中部的 91 种本土植物进行了酪氨酸酶抑制活性研究 [10]。尽管已报道了许多合成酪氨酸酶抑制剂,但只有熊果苷和曲酸等少数几种在商业上得到使用,主要是因为其具有细胞毒性高、穿透力不足、活性低和稳定性低等缺点 [11]。
α-蒎烯与没食子酸对酪氨酸酶活性影响的比较
主要关键词