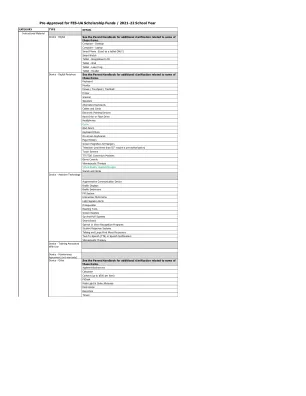
MI Cancer Seek 是第一个也是唯一一个同时进行的基于全外显子组和全转录组且具有成人和儿科患者伴随诊断适应症的检测 德克萨斯州欧文,2024 年 11 月 6 日——领先的下一代 AI TechBio 公司和精准医疗先驱 Caris Life Sciences ® (Caris) 今天宣布,美国食品药品监督管理局 (FDA) 已批准 MI Cancer Seek™ 作为伴随诊断 (CDx) 来识别可能受益于靶向疗法治疗的癌症患者。该检测包括一种泛癌症和五种肿瘤特定适应症,适用于多种 FDA 批准的疗法。MI Cancer Seek 是第一个也是唯一一个同时进行的基于全外显子组测序 (WES) 和全转录组测序 (WTS) 的检测,具有 FDA 批准的 CDx 适应症,可用于实体肿瘤的分子分析。MI Cancer Seek 适用于 1-22 岁的成人和儿科患者。 Caris 董事长、创始人兼首席执行官 David Dean Halbert, DSc (hc) 表示:“FDA 批准 MI Cancer Seek 作为同类产品中的首个,进一步证明了 Caris 在分子科学领域的持续领导地位以及我们对质量的极度关注。我们很高兴将 MI Cancer Seek 推向市场,确保患者能够使用关键的精准医疗工具。” MI Cancer Seek 是一种基于下一代测序 (NGS) 的体外诊断 (IVD) 设备,使用从福尔马林固定石蜡包埋 (FFPE) 肿瘤组织样本中分离的总核酸 (TNA) 来检测 228 个基因中的单核苷酸变异 (SNV) 和插入和缺失 (indel)、微卫星不稳定性 (MSI)、先前诊断为实体瘤的患者的肿瘤突变负担 (TMB) 以及乳腺癌患者一个基因的拷贝数扩增 (CNA)。 MI Cancer Seek 旨在作为一种伴随诊断,根据已获批准的治疗产品标签,识别可能从伴随诊断指征表中所列的靶向治疗中受益的患者。此外,MI Cancer Seek 旨在提供肿瘤突变分析,供合格的医疗保健专业人员根据专业肿瘤学指南为先前诊断为恶性实体肿瘤的癌症患者使用。伴随诊断指征表中未列出的基因组学发现对于任何特定治疗产品的标签使用并非规定性或决定性的。Caris 总裁 David Spetzler(硕士、博士、工商管理硕士)表示:“我们非常高兴我们的 MI Cancer Seek 测试获得 FDA 批准。FDA 对新技术的评估非常严格,确保患者能够接受安全有效的测试。与 FDA 合作的过程既富有协作性又富有见地,我们赞赏他们在评估新技术方面的专业知识。”
Caris Life Sciences 获得 FDA 批准 MI Cancer Seek™
主要关键词